FUNCIONES DE LAS PROTEÍNAS
- Estructural: forman el citoesqueleto. Forman parte de la piel, del pelo, y del tejido conjuntivo de los órganos del cuerpo (parte de los órganos que hace que mantengan su forma y estructura). Ejemplo de proteínas estructurales: colágeno, elastina, queratina.
- Hormonal: las hormonas son los mensajeros y reguladores del cuerpo. Como ejemplo de proteínas que son hormonas tenemos a la insulina y al glucagón (regulan los niveles de azúcar en la sangre, o sea, regulan la glicemia, sacando o "metiendo" glucosa, el monosacárido más simple, a las células), y a la hormona del crecimiento.
- Defensiva: en la sangre, hay moléculas encargadas de digerir a bacterias, pelear contra enfermedades, etc., llamadas anticuerpos. Las proteínas que funcionan como anticuerpos en la sangre son las immunoglobulinas. También, la trombina y el fibrinógeno participan en la coagulación sanguínea (cuando se rompe un vaso sanguíneo y hay que repararlo).
- Transporte: proteínas transportadoras de la membrana plasmática (membrana plasmática=envuelve a la célula, separándola de su medio ambiente. Si la célula fuese una habitación de una casa, la membrana plasmática es las paredes que separan a esa pieza del resto de la casa, y las proteínas transportadoras serían las puertas y las ventanas de la pieza).
- Contráctil: actina y miosina son responsables de la contracción muscular, ej. cuando hacemos deporte.
- Enzimática: son las proteínas más numerosas y especializadas. Catalizan las reacciones químicas dentro de la célula. "Hacen que las cosas pasen".
LÍPIDOS
1. Composición química: C-H-O-P-S (¿a qué átomos corresponden estos símbolos químicos?)
2. Propiedades: no son solubles (no se disuelven) en agua, y otros solventes polares. Presentan un aspecto graso (brillantes, resbalosos si se tocan).
3. Monómeros y polímeros: a diferencia de todas las otras moléculas orgánicas (carbohidratos, proteínas) que hemos visto, los lípidos son un grupo muy heterogéneo (variado) de moléculas. Es decir, pueden tomar numerosas formas, al componerse de un número de estructuras bastante amplio, no como las otras moléculas donde, por ejemplo en el caso de las proteínas, eran puros amino ácidos uno después de otro unidos por un enlace peptídico.
martes, 22 de mayo de 2012
jueves, 10 de mayo de 2012
Clase 4 - Proteínas
Tras haber visto el agua, las sales minerales, y los carbohidratos, las proteínas son la segunda macromolécula orgánica que estudiaremos, dentro de la unidad "Composición Química de los Seres Vivos".
1. Composición química: C-H-O-N-S (¿a qué átomos corresponden estos símbolos químicos?
2. Monómeros y Polímeros
- Los monómeros de las proteínas se llaman amino ácidos o péptidos. Ahora, los amino ácidos están hechos de distintos componentes, o distintos grupos funcionales, como lo muestra el siguiente diagrama:
El ámino ácido tiene, en torno al "C" que vemos en el esquema, llamado carbono central, un grupo amino: NH2, un grupo carboxilo: COOH, un hidrógeno: H, y una cadena lateral o radical: R. Con cadena lateral nos referimos a que, en esa ubicación, se pueden ubicar muchas cosas, desde un simple átomo de hidrógeno, a grandes grupos de átomos.
Existen 20 amino ácidos en total. De estos, el cuerpo humano puede producir sólo 10. O sea, hay otros 10 amino ácidos que el cuerpo NO puede producir por si solo. Por ende, estos los debemos obtener de los alimentos que comemos. Por esto mismo, a los amino ácidos que no podemos producir los llamamos "esenciales": es "esencial" que los comamos (esencial=absolutamente necesario). Los otros 10 amino ácidos, son los amino ácidos no esenciales.
Pregunta de reforzamiento: ¿Qué parte del amino ácido (con parte nos referimos a grupo amino, grupo carboxilo, etc.) va a marcar la diferencia entre los 20 amino ácidos que existen?
- Los polímeros resultan de la unión de los monómeros. Entonces, muchos amino ácidos unidos van a forman a las proteínas, o a los polipéptidos (poli=muchos. Por ende polipéptido quiere decir "muchos péptidos"). Los polipéptidos pueden tener hasta miles de amino ácidos, unidos todos en fila.
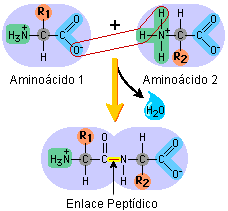
- El proceso de la polimerización forma la unión entre dos monómeros para formar un polímero. En el caso de las proteínas, esta unión (o enlace) se llama enlace peptídico (por péptido). Los amino ácidos no se unen de cualquier manera entre si, si no que lo hacen de manera ordenada. El grupo carboxilo de un amino ácido, se unirá con el grupo amino del otro amino ácido, para poder así formar largas cadenas de amino ácidos. Veamos el siguiente esquema:
Vemos que, cada vez que unimos un amino ácido con otro, por el grupo carboxilo COOH de uno con el grupo amino NH2 del otro, se forma una molécula de agua, H2O.
Resumen: Siguiendo la línea de las clases anteriores, el amino ácido es la pieza chica de lego, que, al juntarse con otros amino ácidos, otras piezas de lego, formarán a las proteínas, que serían pues grandes cadenas de lego. Cuando juntamos las dos piezas de lego, existe entre ellas un enlace peptídico. Si recordamos que en la unión de amino ácidos sólo participa el grupo carboxilo COOH de uno, con el grupo amino NH2 de otro, entonces vemos que las piezas de lego pueden unirse sólo por algunos lados. Digamos que el lado derecho de la pieza de lego es el COOH, y el izquierdo el NH2. Las piezas de lego las iremos juntando lado derecho con lado izquierdo, lado derecho con lado izquierdo. Es decir, la filita de amino ácidos, que es el polipéptido, la iríamos armando de izquierda a derecha.
3. Estructura de las proteínas
- Existen cuatro niveles de estructuración de las proteínas: primario, secundario, terciario, y cuaternario.
- Estructura primaria: la fila de amino ácidos, todos unidos por medio de enlaces peptídicos. Es lo que primero se obtiene, tratando de formar una proteína.
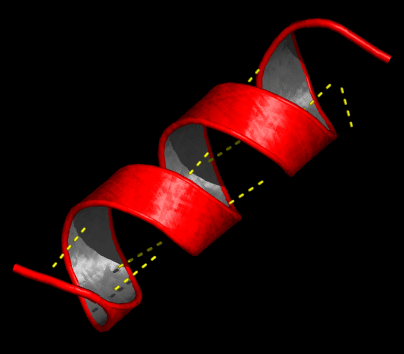
- Estructura secundaria: la fila de amino ácidos se dobla, se plega, sobre si misma, como si enrollamos una cinta alrededor de algo. Pueden formarse dos formas principales: alfa hélice y lámina beta (diagramas abajo)
- Estructura terciaria: la estructura secundaria se sigue doblando.
- Estructura cuaternaria: se unen dos proteínas con estructura terciaria.
O sea, vemos que cada nivel forma proteínas más complejas, más difíciles de ver, que el anterior. Por eso que hablamos de que la estructura que puede adoptar una proteína es como una escalera: del peldaño de más abajo, el primero, se pasa al segundo. Sólo estando en segundo se puede subir al tercero, para después ir al cuarto que es el peldaño de más arriba, o sea, el más complicado.
4. Propiedades de las proteínas
- Desnaturación: Las proteínas pueden perder la estructura de la cual hablamos anteriormente, por diversos factores de desnaturación: pH (si están en un lugar ácido o básico), alzas en la temperatura, o agitación mecánica. La desnaturación funciona de la misma manera que la escalera de la cual hablamos antes, pero en vez de subir peldaños, bajamos peldaños. Si desnaturo una proteína con estructura 4, pasa a ser una proteína de estructura 3. Si desnaturo esta proteína, se convierte en una de estructura 2, y si desnaturo esta también, pasa a ser la proteína de estructura 1.
Pregunta de reforzamiento: si sabemos que "desnaturar" es lo mismo que "perder la estructura", ¿podemos desnaturar una proteína de estructura primaria? (pensar: ¿a qué escalón se iría?).
1. Composición química: C-H-O-N-S (¿a qué átomos corresponden estos símbolos químicos?
2. Monómeros y Polímeros
- Los monómeros de las proteínas se llaman amino ácidos o péptidos. Ahora, los amino ácidos están hechos de distintos componentes, o distintos grupos funcionales, como lo muestra el siguiente diagrama:
El ámino ácido tiene, en torno al "C" que vemos en el esquema, llamado carbono central, un grupo amino: NH2, un grupo carboxilo: COOH, un hidrógeno: H, y una cadena lateral o radical: R. Con cadena lateral nos referimos a que, en esa ubicación, se pueden ubicar muchas cosas, desde un simple átomo de hidrógeno, a grandes grupos de átomos.
Existen 20 amino ácidos en total. De estos, el cuerpo humano puede producir sólo 10. O sea, hay otros 10 amino ácidos que el cuerpo NO puede producir por si solo. Por ende, estos los debemos obtener de los alimentos que comemos. Por esto mismo, a los amino ácidos que no podemos producir los llamamos "esenciales": es "esencial" que los comamos (esencial=absolutamente necesario). Los otros 10 amino ácidos, son los amino ácidos no esenciales.
Pregunta de reforzamiento: ¿Qué parte del amino ácido (con parte nos referimos a grupo amino, grupo carboxilo, etc.) va a marcar la diferencia entre los 20 amino ácidos que existen?
- Los polímeros resultan de la unión de los monómeros. Entonces, muchos amino ácidos unidos van a forman a las proteínas, o a los polipéptidos (poli=muchos. Por ende polipéptido quiere decir "muchos péptidos"). Los polipéptidos pueden tener hasta miles de amino ácidos, unidos todos en fila.
- El proceso de la polimerización forma la unión entre dos monómeros para formar un polímero. En el caso de las proteínas, esta unión (o enlace) se llama enlace peptídico (por péptido). Los amino ácidos no se unen de cualquier manera entre si, si no que lo hacen de manera ordenada. El grupo carboxilo de un amino ácido, se unirá con el grupo amino del otro amino ácido, para poder así formar largas cadenas de amino ácidos. Veamos el siguiente esquema:
Vemos que, cada vez que unimos un amino ácido con otro, por el grupo carboxilo COOH de uno con el grupo amino NH2 del otro, se forma una molécula de agua, H2O.
Resumen: Siguiendo la línea de las clases anteriores, el amino ácido es la pieza chica de lego, que, al juntarse con otros amino ácidos, otras piezas de lego, formarán a las proteínas, que serían pues grandes cadenas de lego. Cuando juntamos las dos piezas de lego, existe entre ellas un enlace peptídico. Si recordamos que en la unión de amino ácidos sólo participa el grupo carboxilo COOH de uno, con el grupo amino NH2 de otro, entonces vemos que las piezas de lego pueden unirse sólo por algunos lados. Digamos que el lado derecho de la pieza de lego es el COOH, y el izquierdo el NH2. Las piezas de lego las iremos juntando lado derecho con lado izquierdo, lado derecho con lado izquierdo. Es decir, la filita de amino ácidos, que es el polipéptido, la iríamos armando de izquierda a derecha.
3. Estructura de las proteínas
- Existen cuatro niveles de estructuración de las proteínas: primario, secundario, terciario, y cuaternario.
- Estructura primaria: la fila de amino ácidos, todos unidos por medio de enlaces peptídicos. Es lo que primero se obtiene, tratando de formar una proteína.
- Estructura secundaria: la fila de amino ácidos se dobla, se plega, sobre si misma, como si enrollamos una cinta alrededor de algo. Pueden formarse dos formas principales: alfa hélice y lámina beta (diagramas abajo)
- Estructura terciaria: la estructura secundaria se sigue doblando.
- Estructura cuaternaria: se unen dos proteínas con estructura terciaria.
O sea, vemos que cada nivel forma proteínas más complejas, más difíciles de ver, que el anterior. Por eso que hablamos de que la estructura que puede adoptar una proteína es como una escalera: del peldaño de más abajo, el primero, se pasa al segundo. Sólo estando en segundo se puede subir al tercero, para después ir al cuarto que es el peldaño de más arriba, o sea, el más complicado.
4. Propiedades de las proteínas
- Desnaturación: Las proteínas pueden perder la estructura de la cual hablamos anteriormente, por diversos factores de desnaturación: pH (si están en un lugar ácido o básico), alzas en la temperatura, o agitación mecánica. La desnaturación funciona de la misma manera que la escalera de la cual hablamos antes, pero en vez de subir peldaños, bajamos peldaños. Si desnaturo una proteína con estructura 4, pasa a ser una proteína de estructura 3. Si desnaturo esta proteína, se convierte en una de estructura 2, y si desnaturo esta también, pasa a ser la proteína de estructura 1.
Pregunta de reforzamiento: si sabemos que "desnaturar" es lo mismo que "perder la estructura", ¿podemos desnaturar una proteína de estructura primaria? (pensar: ¿a qué escalón se iría?).
jueves, 3 de mayo de 2012
Clase 3 - Carbohidratos
De la clase anterior, sabemos que los carbohidratos se forman a partir de monómeros que llamaremos monosacáridos, los cuales se van juntando, como lo harían las piezas de un lego, para crear compuestos más y más grandes.
1. Disacáridos = dos monosacáridos. Cada disacárido se encuentra en distintos lugares, con funciones únicas. Las diferencias entre disacáridos son debido a los monosacáridos que los componen. Siguiendo con el ejemplo del lego, donde los monosacáridos son las piezas más chicas de un lego, si juntamos una pieza verde con una verde, el resultado será distinto a haber juntado la misma primera pieza verde con una pieza amarilla. Algunos de los disacáridos más comunes son:
- Maltosa = glucosa + glucosa. Se encuentra en semillas.
- Sacarosa = glucosa + fructosa. Es el "azúcar de mesa", y proviene de la remolacha y de la caña de azúcar.
- Lactosa = glucosa + galactosa. Es el azúcar de la leche.
Recordemos las funciones de los carbohidratos: energía a corto plazo (para ocupar inmediatamente, como cuando nos comemos un chocolate antes de una prueba), energía a largo plazo (o sea, que se guarda en el cuerpo para cuando sea necesaria), y formar parte de estructuras (como la madera en los árboles, o la concha de un cangrejo). Los disacáridos, por ser estructuras simples y pequeñas, no van a cumplir tareas tan complicadas como ser parte de una estructura, o formar parte de nuestra reserva energética. Entonces, su principal función es ser fuente de energía a corto plazo.
2. Oligosacáridos = entre 2 y 10 monosacáridos juntos. Por ende, son más grandes que los disacáridos, pudiendo cumplir entonces funciones más complejas.
3. Polisacáridos = muchos monosacáridos juntos. Son más grandes que los disacáridos, y que los oligosacáridos. Por lo mismo, pueden cumplir tareas complejas en los seres vivos, como ser los principales componentes de la madera, de los esqueletos de algunos animales, etc. Teniendo en mente estas funciones ya dichas, podemos dividir a los polisacáridos en dos grandes grupos: polisacáridos de reserva energética (su función es guardar energía en los organismos), y polisacáridos estructurales.
Algunos de los polisacáridos de reserva energética más comunes son:
- Almidón = muchas glucosas. Se encuentra en las plantas, ejemplo: papas, trigo, maíz, etc.
- Glucógeno = muchas glucosas. Se encuentra en animales, principamente en el hígado.
- Pregunta de reforzamiento: ¿podemos encontrar glucógeno en una planta? ¿Por qué sí, o por qué no?
Algunos de los polisacáridos de estructura más comunes son:
- Celulosa = muchas glucosas. Se encuentra en la pared celular de las células vegetales, aportando rigidez, ejemplo: madera.
- Quitina = muchas glucosas. Se encuentra en las células de animales, como los cangrejos.
Muchos se preguntarán cómo puede ser la celulosa distinta de la quitina, o la celulosa distinta del almidón o el almidón distinto del glucógeno, si todos están hechos de glucosa. Esto puede responderse nuevamente con el ejemplo del lego. Imaginemos que todas las glucosas son piezas de lego rojas. Si yo pongo una pieza roja encima de otra, y otra más encima, y otra y otra, obtengo una torre roja. Pero también, puedo empezar a poner piezas para el lado, y ya no me queda una torre, si no otra forma. Y puedo empezar a poner piezas por donde quiera y me pueden salir muchas formas distintas. Lo mismo pasa cuando se juntan muchas glucosas: se pueden juntar de muchas formas distintas, logrando los distintos compuestos que hemos analizado.
1. Disacáridos = dos monosacáridos. Cada disacárido se encuentra en distintos lugares, con funciones únicas. Las diferencias entre disacáridos son debido a los monosacáridos que los componen. Siguiendo con el ejemplo del lego, donde los monosacáridos son las piezas más chicas de un lego, si juntamos una pieza verde con una verde, el resultado será distinto a haber juntado la misma primera pieza verde con una pieza amarilla. Algunos de los disacáridos más comunes son:
- Maltosa = glucosa + glucosa. Se encuentra en semillas.
- Sacarosa = glucosa + fructosa. Es el "azúcar de mesa", y proviene de la remolacha y de la caña de azúcar.
- Lactosa = glucosa + galactosa. Es el azúcar de la leche.
Recordemos las funciones de los carbohidratos: energía a corto plazo (para ocupar inmediatamente, como cuando nos comemos un chocolate antes de una prueba), energía a largo plazo (o sea, que se guarda en el cuerpo para cuando sea necesaria), y formar parte de estructuras (como la madera en los árboles, o la concha de un cangrejo). Los disacáridos, por ser estructuras simples y pequeñas, no van a cumplir tareas tan complicadas como ser parte de una estructura, o formar parte de nuestra reserva energética. Entonces, su principal función es ser fuente de energía a corto plazo.
2. Oligosacáridos = entre 2 y 10 monosacáridos juntos. Por ende, son más grandes que los disacáridos, pudiendo cumplir entonces funciones más complejas.
3. Polisacáridos = muchos monosacáridos juntos. Son más grandes que los disacáridos, y que los oligosacáridos. Por lo mismo, pueden cumplir tareas complejas en los seres vivos, como ser los principales componentes de la madera, de los esqueletos de algunos animales, etc. Teniendo en mente estas funciones ya dichas, podemos dividir a los polisacáridos en dos grandes grupos: polisacáridos de reserva energética (su función es guardar energía en los organismos), y polisacáridos estructurales.
Algunos de los polisacáridos de reserva energética más comunes son:
- Almidón = muchas glucosas. Se encuentra en las plantas, ejemplo: papas, trigo, maíz, etc.
- Glucógeno = muchas glucosas. Se encuentra en animales, principamente en el hígado.
- Pregunta de reforzamiento: ¿podemos encontrar glucógeno en una planta? ¿Por qué sí, o por qué no?
Algunos de los polisacáridos de estructura más comunes son:
- Celulosa = muchas glucosas. Se encuentra en la pared celular de las células vegetales, aportando rigidez, ejemplo: madera.
- Quitina = muchas glucosas. Se encuentra en las células de animales, como los cangrejos.
Muchos se preguntarán cómo puede ser la celulosa distinta de la quitina, o la celulosa distinta del almidón o el almidón distinto del glucógeno, si todos están hechos de glucosa. Esto puede responderse nuevamente con el ejemplo del lego. Imaginemos que todas las glucosas son piezas de lego rojas. Si yo pongo una pieza roja encima de otra, y otra más encima, y otra y otra, obtengo una torre roja. Pero también, puedo empezar a poner piezas para el lado, y ya no me queda una torre, si no otra forma. Y puedo empezar a poner piezas por donde quiera y me pueden salir muchas formas distintas. Lo mismo pasa cuando se juntan muchas glucosas: se pueden juntar de muchas formas distintas, logrando los distintos compuestos que hemos analizado.
Suscribirse a:
Entradas (Atom)